CART 细胞治疗是一种非常有前景的癌症治疗方法。目前被广泛应用于血液肿瘤中。大部分晚期癌症最终进展为常规治疗难治性疾病,需要新的治疗模 式。免疫疗法增强基于对抗肿瘤的免疫应答,是治疗很多癌症类型的非常有前景的方法。在破坏全身患病细胞中,T 细胞具有重要作用。免疫检查点抑制剂和肿瘤浸润淋巴细胞的研究表明了 T 细胞治疗癌症的潜力。T 细胞需要适当的肿瘤特异性,有足够的数量,并且克服任何局部免疫抑制因素,才能有效。工程化自体细胞疗法(eACT™)是患者自身的 T 细胞聚集,并且随后发生遗传改变,能够识别并靶向特定恶性肿瘤细胞表面表达的抗原的一个过程。
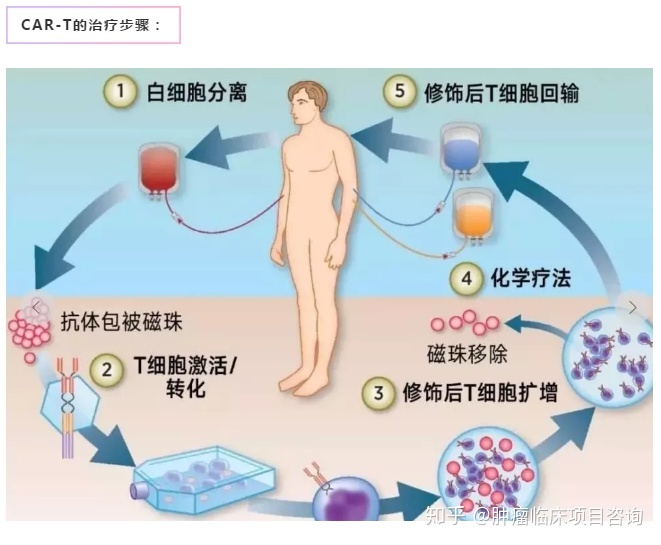
1.从癌症病人身上分离免疫T细胞;
2.利用基因工程技术,通过逆转录病毒和慢病毒载体、转座系统(如SB 转座系统)或直接将mRNA转导到T细胞内,使T细胞表面表达嵌和抗原受体(CAR),即成为CAR-T细胞,拥有识别癌细胞和增殖的作用;
3.体外扩增CAR-T细胞,一般一个病人需要几十亿,乃至上百亿个CAR-T细胞(体型越大需要细胞越多);
4.把扩增好的CAR-T细胞输回病人体内;
5.严密监控病人,尤其是控制前几天身体的剧烈反应。
本项目CART 细胞产品通过成熟的 T 细胞诱导改造技术,构建起针对肿瘤靶点的 CART 细胞,并通过流式细胞技术鉴定其为靶向 CAR+细胞。利用针对肿瘤靶点的 CART 细胞、未改造的 T 细胞分别和肿瘤靶点阳性的靶细胞共培养的细胞杀伤实验证明,一段时间后收集上清进行检测。我们发现 CART 细胞而非未改造的 T 细胞在应对肿瘤靶点阳性的靶细胞时释放了大量的 IFNγ。这表明制作的针对肿瘤靶点阳性的 CART 细胞可以特异性识别 肿瘤靶点阳性靶细胞,并通过大量释放 IFN γ 来激活 T 细胞功能,实现肿瘤杀伤。
本项目中用到的 CART 细胞可以在体内被迅速激活并扩增,本项目的 CART 细胞是利用人源化抗体构建起 CAR 分子,以此避免人抗鼠效应对基于鼠源抗体的 CART 细胞功能的影响,使其更好发挥功能的同时,并延长其持续时间。
CAR-T疗法是当今最火热的免疫治疗之一,也是近十年来免疫医学的重大突破。它是通过对患者自身的免疫细胞T进行基因改造,从而使被改造过的T淋巴细胞能够精准对抗患者体内癌细胞的一种细胞免疫治疗。CAR-T细胞疗法目前针对的主要是血液恶性肿瘤,包括急性B淋巴细胞白血病,B细胞淋巴瘤和多发性骨髓瘤等。尽管CART疗法在治疗实体瘤上也有个别成功病例的报道,但总体疗效不尽如人意, 其中一大障碍就是因为实体瘤的肿瘤微环境抑制了CAR-T的功能,从而使CAR-T丧失了对肿瘤细胞的杀伤能力。目前众多科研工作者致力于CAR-T的改造和优化,希望通过寻找最佳肿瘤靶向、保持T细胞的体内持久性和抵抗肿瘤微环境的免疫抑制等途径以提高其疗效。我们相信在不久的将来这一疗法在实体瘤上会取得突破性的进展。
目前在国外上市两款CAR-T产品分别是诺华公司的Kymaiah和KitePharma公司的Yescarta,用于治疗青少年急性B淋巴细胞白血病和大B细胞淋巴瘤,但其价格昂贵,分别为47.5万美元和37.5万美元(相当于人民币200万以上)。在国内目前CAR-T疗法还处于临床试验阶段,其中治疗范围集中在以下领域:
1. 一线或二线治疗失败的B细胞非霍奇金淋巴瘤,包括弥漫大B细胞淋巴瘤,套细胞淋巴瘤和滤泡淋巴瘤等。
2. 难治复发的多发性骨髓瘤。
3. 难治复发(包括移植后复发)的急性B系淋巴细胞白血病。
CAR-T的治疗流程
1) 治疗前2-3周,提取患者T细胞(患者):采集患者外周静脉血60~100ml;或使用机器单采患者50ml左右单个核细胞悬液,单采一般耗时在1.5-2.5小时左右。
2) 体外制备CAR-T细胞(GMP实验室;实验人员操作):经过体外分离和纯化T细胞,然后通过慢病毒转导等方式使得分离纯化的T细胞表达嵌合抗原受体(CAR),即成为CAR-T细胞,然后扩增到用于临床治疗的CAR-T细胞数量。这个制备过程所需的时间因不同的细胞产品而不同,一般1-3周左右。
3)治疗前1周左右,CAR-T治疗前的预处理化疗(患者):患者细胞治疗前接受适当的化疗,以减少体内肿瘤细胞数量,达到“清淋”的程度,同时提高CAR-T细胞的疗效。化疗将开始于抗CD19 CAR-T细胞回输前5~10天,进而保证在CAR-T细胞回输前的1~2天完成化疗。
4) CAR-T细胞回输(患者):采用剂量单次或分次通过静脉输注(20分钟左右),将制备好的CART细胞回输给患者。回输结束后在规定的时间评估点进行检查,评估疗效及毒副反应。
简而言之,CART细胞治疗就是在先提取患者的T细胞,然后在GMP实验室操作人员通过基因编辑技术把靶向肿瘤细胞的CAR装到患者T细胞身上,成为CART细胞;然后把CART回输给患者。